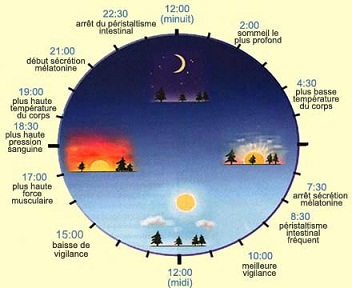
Les rouages de l’horloge biologique
Tous les organismes vivant sur la Terre, y compris l’être humain, sont le fruit d’une longue évolution. Or, cette évolution est depuis toujours soumise au rythme du jour et de la nuit causé par la rotation de la Terre sur elle-même.
Il était donc prévisible que quelque chose ait évolué dans notre organisme pour coordonner ses grandes fonctions avec les différents moments de la journée. La vigilance, la température corporelle ou la sécrétion de certaines hormones gagne en effet à être ajustée selon qu’il fait jour ou qu’il fait nuit.
Les premiers indices d’une telle « horloge biologique » sont venues des études de volontaires qui sont restés plusieurs semaines coupés de tout indicateur du jour et de la nuit (souvent en campant dans des grottes). Or, dans ces conditions, un rythme d’environ 24 heures persiste tant dans les comportements que dans les paramètres physiologiques de ces individus.
Des variations cycliques se maintiennent même à l’intérieur de cellules du corps humain isolées dans un milieu de culture soumis à un éclairage constant. L’activité de certains gènes et la sécrétion de certaines substances continuent de fluctuer selon un rythme de plus ou moins 24 heures.
Notre horloge biologique réside donc au cœur même de nos cellules et ses rouages ne sont pas faits de ressorts et de roues dentelées, mais bien de molécules. Lesquelles, et comment interagissent-elles pour maintenir des cycles de 24 heures ? Difficile question qu’on n’a commencé à répondre qu’au début des années 1970 avec la découverte chez la mouche drosophile du premier gènes impliqué dans l’horloge biologique.
Difficulté d’autant plus grande qu’on s’est rendu compte que chaque espèce possède des variantes qui lui sont propres. L’horloge biologique humaine possède par exemple certaines molécules qui sont les mêmes que l’horloge biologique de la mouche drosophile, mais aussi d’autres qui lui sont propres. Mais dans tous les cas, l’horloge fonctionne grâce à ce qu’on appelle couramment une boucle de rétroaction négative.
Le point de départ de cette boucle, ce sont des gènes, donc des bouts d’ADN qui fournissent les plans pour fabriquer des protéines. Ces plans sont transmis du gène au cytoplasme, lieu de production des protéines, par une molécule appelée ARN messager (ou ARNm). Mais alors que la plupart des protéines demeurent habituellement dans le cytoplasme où elles remplissent différentes fonctions (on les appellent parfois « les briques du vivant »), celles qui sont impliquées dans notre horloge biologique retournent dans le noyau où se trouvent l’ADN et se fixent sur le gène qui les a produites. Ce faisant, elles arrêtent l’activité de leur propre gène. Moins de protéines sont alors fabriquées, si bien qu’à un moment donné, il n’y a plus assez de protéines qui retournent dans le noyau pour empêcher leur production et celle-ci reprend. Environ 24 heures se sont alors écoulées. Les protéines commencent ensuite à s’accumuler à nouveau, initiant du même coup un nouveau cycle.
Les cellules ganglionnaires photosensibles
Dès que l’on s’est aperçu que notre horloge biologique centrale, située dans le noyau suprachiasmatique de l’hypothalamus, a besoin d’être resynchronisée quotidiennement par la lumière du jour, on a suspecté les photorécepteurs du système visuel d’être à l’origine de ce photo-entraînement.
C’est donc avec un certain étonnement que plusieurs équipes travaillant sur le rythme circadien en arrivèrent à la conclusion, au début des années 2000, qu’il existait un autre système photosensible chez l’être humain. Cet autre système était non pas dédié à la vision mais servait plutôt à déterminer l’intensité lumineuse générale. Exactement comme le fait le posemètre d’un appareil photo dont la fonction n’est pas de fixer avec précision l’image, mais de déterminer le bon temps d’exposition en fonction de l’intensité lumineuse disponible.
Différentes expériences montrèrent assez vite que ce nouveau système n’utilisait pas ou alors très peu les photopigments connus à l’époque, soit la rhodopsine des bâtonnets et les différentes opsines des cônes. Il utilisait plutôt la mélanopsine et/ou le cryptochrome, deux protéines photosensibles dont l’implication dans ce nouveau système est encore débattue.
Autre surprise, les cellules qui contiennent ces nouveaux pigments photosensibles ne sont ni les cônes ni les bâtonnets de la rétine, mais bien certaines cellules ganglionnaires. Surprenant parce que ces cellules n’étaient reconnues que pour intégrer et exporter le signal lumineux hors de l’œil grâce à leur axone qui forme le nerf optique. Elles n’avaient donc jamais été suspectées de capacités photoréceptrices ni de propriétés électrophysiologiques adaptées à la détection de l’intensité lumineuse ambiante.
Il s’agit en fait d’un sous-groupe de cellules ganglionnaires possédant de longues dendrites couvrant de larges portions de la rétine et un axone (indiqué par la flèche sur le dessin ci-contre) qui rejoint le noyau suprachiasmatique de l’hypothalamus.
Le noyau suprachiasmatique et la glande pinéale
La plupart de nos comportements et des grandes fonctions de notre organisme ne sont pas constants mais fluctuent selon un horaire de 24 heures. On n’a qu’à penser au cycle de veille et de sommeil, à celui de la température corporelle, de l’appétit ou encore au moment où sont sécrétées nos différentes hormones.
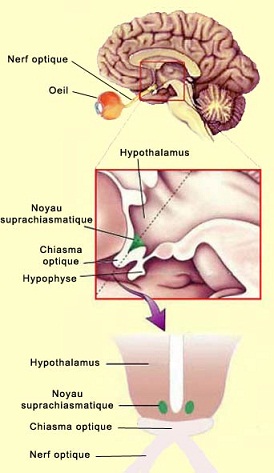
On connaît l’emplacement de l’horloge centrale qui régule l’ensemble de ces cycles circadiens. Il s’agit de deux minuscules structures cérébrales pas plus grosse que la pointe d’un crayon. Elle comprennent quelques dizaines de milliers de neurones chacune et sont situées à la base de l’hypothalamus. On les appelle noyaux suprachiasmatiques (NSC) parce qu’ils sont également situés juste au-dessus du chiasma optique, l’endroit où les deux nerfs optiques se croisent.
Cette position stratégique permet aux noyaux suprachiasmatiques de recevoir des prolongements du nerf optique qui lui indique le niveau d’intensité lumineuse ambiante. Leurs neurones peuvent ainsi se resynchroniser quotidiennement avec la lumière du jour. Car comme n’importe quelle horloge, notre horloge biologique n’est pas parfaite et doit ainsi être ajustée quotidiennement.
Cela dit, il s’agit bel et bien d’une horloge ayant un rythme autonome car plusieurs expériences ont démontré que les variations de notre cycle circadien persistent chez les individus isolés de la lumière du jour. Et lorsqu’on détruit les noyaux suprachiasmatiques chez le hamster par exemple, on désorganise complètement ses activités rythmiques comme l’alternance veille-sommeil. De même, si on prélève ces noyaux d’un foetus de hamster pour les transplanter à l’animal lésé, on rétablit les rythmes, mais avec les propriétés du donneur.
Cela indique que le mécanisme de notre horloge biologique est non seulement bel et bien endogène, mais également d’origine génétique. Et de fait, on sait maintenant que ces rythmes sont le fruit de l’activité cyclique de certains gènes.
Les voies de sortie du noyau suprachiasmatique lui permettent ensuite d’ajuster les cycles de plusieurs fonctions physiologiques et comportementales. Les axones qui en sont issus innervent principalement l’hypothalamus et des structures proches. Certains vont aussi rejoindre d’autres parties du diencéphale et d’autres encore se rendent jusqu’au mésencéphale.
Enfin, une structure très importante reçoit des signaux du NSC, bien que de manière indirecte : il s’agit de la glande pinéale (aussi appelée épiphyse). Chez les oiseaux, les reptiles et les poissons, cette petite glande située au sommet du cerveau est sensible à la lumière et coordonne elle-même des phénomènes cycliques chez ces animaux. Chez les mammifères toutefois, bien que la glande pinéale conserve sa capacité de synthétiser de façon cyclique, en l’occurrence la nuit, l’hormone mélatonine, elle ne constitue pas en elle-même une horloge et la synthèse cyclique de l’hormone est dépendante des signaux du NSC.
La mélatonine, parfois appelée « l’hormone du sommeil », commence à être produite par la glande pinéale à la tombée du jour. Quand le niveau sanguin de l’hormone s’élève, la température corporelle baisse légèrement et le besoin de dormir se fait de plus en plus sentir. Ce niveau reste élevé pendant à peu près 12 heures, puis redescend en début de matinée quand la lumière du jour inhibe l’activité de la glande pinéale.
Si l’on revient à notre horloge centrale située dans le NSC, on ne sait pas encore dans le détail comment elle règle tant de comportements cycliques dans l’organisme. Mais on sait qu’elle met à contribution la glande pinéale et on a pu montrer qu’en détruisant les efférences du NSC, on supprime également les rythmes circadiens.
Le GABA étant le neurotransmetteur essentiel de pratiquement tous les neurones du NSC, on peut s’attendre à un effet inhibiteur sur les neurones qu’ils innervent. En plus de ces voies axonales véhiculant les messages de sortie, il semblerait que les neurones du NSC sécrètent avec une certaine rythmicité de la vasopressine, un peptide neuromodulateur. On a d’ailleurs démontré que cette sécrétion cyclique découlait du fait que la région promotrice du gène de la vasopressine (son interrupteur, en quelque sorte) était contrôlée par les mêmes protéines qui règlent les boucles de rétroaction génétiques de base de notre horloge moléculaire. Mentionnons enfin que les effets de cette vasopressine sécrétée par les neurones du NSC sont uniquement cérébraux, contrairement à la vasopressine hypophysaire impliquée dans le métabolisme de l’eau pour l’ensemble de l’organisme.
L’hormone sécrétée par la glande pinéale, la mélatonine, ne fut découverte que vers la fin des années 1950. Le rôle de cette hormone dans les rythmes biologiques se dévoila ensuite progressivement. La glande pinéale fut ainsi la dernière des glandes endocrines dont la fonction fut identifiée.
La chronobiologie
Notre environnement naturel est fait de rythmes et d’événements cycliques dont l’origine ultime remonte à l’agencement particulier de notre système solaire. Ainsi, températures et précipitations fluctuent au rythme des saisons. Celles-ci découlent de la révolution annuelle de la terre autour de soleil et de l’inclinaison de l’axe de rotation de la terre sur elle-même. D’autres phénomènes, comme les marées, dépendent de la révolution mensuelle de la lune autour de la terre. Sans parler évidemment de l’alternance du jour et de la nuit causée par la rotation de la terre sur elle-même en 24 heures.
Le cerveau ayant évolué dans cet environnement cyclique depuis toujours, il s’y est adapté de multiples façons. Le plus évident est le cycle éveil sommeil qui suit celui de l’alternance du jour et de la nuit. Mais il peut aussi orchestrer des comportements cycliques sur de longues périodes, comme l’hibernation par exemple. Ou sur des périodes beaucoup plus courte que la journée, comme le cycle respiratoire. Le cortex cérébral lui-même présente des rythmes qui ont des périodes encore plus courtes pouvant atteindre des dizaines de cycles par seconde.
Les rythmes sont donc omniprésents dans le système nerveux des mammifères allant de presque 100 fois par seconde (ou 100 Hertz) pour les EEG corticaux à une seule fois dans l’année (ou 0,00000003 Hz !) pour de nombreux comportements saisonniers tels que l’accouplement du cerf à l’automne, l’hibernation, etc.
L’étude de ces rythmes biologiques dans l’organisme s’appelle la chronobiologie. En attirant l’attention sur la dimension temporelle de nos activités physiologiques et psychologiques, la chronobiologie a permis de mieux comprendre plusieurs phénomènes, entres autres pourquoi certains médicaments sont plus efficaces lorsqu’ils sont pris à des moments particuliers de la journée.
La chronobiologie nous parle de rythmes ou de cycles, c’est-à-dire de phénomènes qui passent par un sommet et un creux au cours d’une certaine période. Comme on l’a dit, la durée de cette période peut varier grandement. On classe généralement les rythmes biologiques en trois grandes catégories selon leur période, soit l’intervalle de temps séparant deux pics ou deux creux au cours d’un cycle.
Les comportements de presque tous les animaux terrestres suivent des rythmes d’origine endogène. Ces rythmes sont également modulés par les variations quotidiennes de lumière et d’obscurité. On appelle ces modifications comportementales cycliques, auxquelles les humains ne font pas exception, les rythmes circadiens.
Les rythmes circadiens sont donc des cycles biochimiques, physiologiques et comportementaux qui oscillent selon une périodicité d’environ 24 heures. Ils sont coordonnés par un oscillateur moléculaire situé dans les neurones du noyau suprachiasmatique. Cette horloge demeure synchronisée avec la l’alternance du jour et de la nuit par l’entremise de cellules rétiniennes spécialisées.
Ce processus d’entraînement de notre horloge biologique avec la lumière du jour est nécessaire parce que le rythme endogène de notre horloge n’est pas exactement de 24h. En effet plusieurs expériences en isolement temporel complet (c’est-à-dire en dehors de tout repère lumineux ou sonore du moment de la journée) ont montré que notre cycle naturel se situait plutôt entre 24,2 et 25,5 heures, selon les études. La racine latine du mot circadien (circa, environ, et dies, jour) prend ici tout son sens, puisque c’est cet entraînement lumineux qui permet à notre horloge centrale de suivre avec précision l’alternance du jour et de la nuit.
Cette horloge centrale coordonne l’activité de nombreuses horloges situées dans différents tissus périphériques et possédant eux aussi leurs propres oscillateurs moléculaires. Voilà pourquoi l’activité de la plupart des grands systèmes physiologiques de l’organisme fluctue selon le moment de la journée. C’est le cas par exemple de la température du corps, du niveau des hormones, de la production d’urine, de la circulation sanguine, du métabolisme et même de la pousse de cheveux !
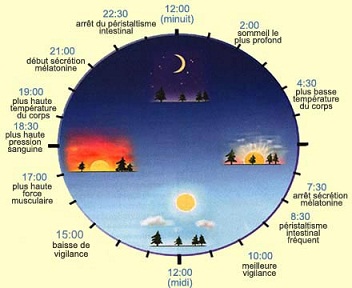
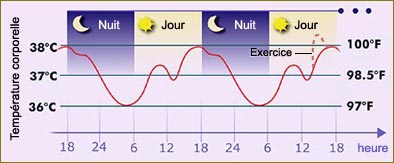
Ces fluctuations passent habituellement par un maximum et un minimum qui coïncident avec une période particulière de la journée. La température corporelle est par exemple toujours la plus basse durant la nuit.
Bien sûr, la température de notre corps peut aussi fluctuer selon des facteurs extérieurs comme le degré d’activité physique, une infection, un stress ou simplement la température ambiante. Mais si l’on garde une personne couchée (mais éveillée) pendant une trentaine d’heures ou plus, on observe également une variation endogène de sa température. Outre le grand creux de la nuit, notre température baisse aussi légèrement du début au milieu de l’après-midi. C’est cette baisse de température endogène, beaucoup plus que la prise du repas du midi, qui expliquerait la baisse de vigilance et même la somnolence ressentie à ce moment de la journée.
D’autres paramètres physiologiques connaissent des fluctuations endogènes importantes au cours de la journée. C’est le cas de la sécrétion de plusieurs hormones. La mélatonine, fabriquée dans la glande pinéale, est presque indécelable dans le sang pendant la journée. Elle commence à être sécrétée en milieu de soirée, à mesure que la lumière diminue, et atteint son pic de sécrétion entre 2 heures et 4 heures du matin.
Le cortisol, dont la sécrétion connaît une pointe juste avant le réveil, atteint son taux le plus élevé au lever et contribue ainsi à l’activation générale de l’organisme.
Le sommeil lent profond, qui survient surtout en début de nuit, est le moment privilégié de la sécrétion de l’hormone de croissance, indispensable pour faire pousser les os et les muscles des enfants. Chez l’adulte, cette hormone a un rôle important dans le métabolisme (favorise la synthèse des protéines, aide à brûler les graisses, diminue la fragilité des os, etc).
La vigilance et la somnolence sont deux aspects d’un même état fluctuant dont les variations circadiennes sont divisées en deux sous-cycles d’environ 12 heures chacun. En d’autres termes, les gens placés dans un environnement dépourvu de repères temporels montrent un rythme biquotidien de propension au sommeil.
La première et la plus importante période de somnolence se manifeste autour de l’heure à laquelle on a l’habitude de se coucher et atteint un sommet entre 3 h et 6 h. C’est l’heure où le métabolisme et la température corporelle ont leur niveau le plus bas. La vigilance est au plus bas, on est physiquement maladroit et on a l’esprit engourdi.
Le deuxième pic de somnolence survient 12 heures plus tard, entre 14 h et 16 h. De moindre importance que le premier, il est néanmoins bien connu de tous : c’est le « coup de fatigue » de milieu d’après-midi. Associé à tort à la digestion du repas du midi, il n’est pas non plus lié à la chaleur de l’après-midi. Des études ont en effet démontré la présence des deux creux dans la courbe de notre vigilance tant chez des sujets vivant sous l’équateur que chez ceux vivant en Amérique du Nord. La somnolence de l’après-midi est également ressentie même si on n’a rien mangé à l’heure du dîner. De plus, chez la plupart des gens, il n’y a pas de somnolence similaire après le déjeuner ou le souper.
Les fluctuations de notre vigilance dépendent donc bel et bien de notre horloge biologique interne. Et une courte sieste l’après-midi serait bénéfique pour la plupart des gens.
Le décalage horaire
Quels processus physiologiques sont derrière les nombreux symptômes désagréables ressentis par les gens qui franchissent en avion plusieurs fuseaux horaires ? Notre compréhension des causes du décalage horaire s’appuie sur le fait qu’il y a dans le corps non pas une mais plusieurs horloges biologiques réparties dans les différents tissus de l’organisme.
Toutes ont des gènes dont les protéines font des boucles de rétroaction négative leur conférant des propriétés oscillatoires endogènes. Ces cycles endogènes dont la durée est proche de 24 heures (d’où l’expression rythmes circadiens) sont normalement entraînés à suivre le rythme du jour et de la nuit grâce à divers facteurs d’entraînement dont la lumière est le principal.
Chez l’humain, l’intensité lumineuse influence directement le noyau suprachiasmatique (ou NSC) par l’entremise de certaines cellules ganglionnaires de la rétine. Le NSC reçoit donc un entraînement direct de la lumière et est considéré comme le chef d’orchestre sur lequel vont s’ajuster toutes les autres horloges. Cette synchronisation des horloges périphériques peut se faire de différentes façons selon les tissus, parfois rapidement par le système nerveux autonome, ou bien plus lentement par voie humorale (glucocorticoïdes, ACTH, etc).
L’une des hypothèses pour expliquer les effets du décalage horaire est qu’il y aurait un déphasage entre nos différentes horloges, déphasage causé par un délai plus où moins long dans la resynchronisation avec les indices lumineux du nouveau fuseau horaire. L’horloge centrale du NSC se resynchronise en effet rapidement après un changement abrupt dans le cycle lumineux. Mais les horloges périphériques seraient beaucoup plus lentes à s’ajuster. Le délai nécessaire aux signaux émis par le NSC pour rejoindre leurs cibles en périphérie pourrait contribuer à cette désynchronisation de l’ensemble. Des expériences chez la souris ont permis de confirmer ce découplage des horloges périphériques de l’horloge centrale lors d’un changement soudain dans la régularité d’un facteur entraînant comme la prise alimentaire ou la lumière.
Des travaux chez le rat laissent aussi entrevoir une autre source de décalage possible pour la désynchronisation des horloges. Chez ce rongeur, on a pu démontrer que l’entraînement lumineux se faisait beaucoup plus rapidement dans le NSC ventral que dans le NSC dorsal. En effet, à l’instar d’autres structures cérébrales, plusieurs sous-régions sont maintenant connues dans les noyaux suprachiasmatiques. Et la région ventrale, celle qui reçoit directement les afférences des cellules ganglionnaires de la rétine, semble être resynchronisée beaucoup plus rapidement par un changement brusque de luminosité.
Il pourrait donc y avoir un décalage qui se produit entre le NSC ventral et dorsal, donc à l’intérieur même de l’horloge centrale. Concrètement, cela veut dire que les horloges périphériques recevant des signaux du NSC seront exposées pendant plusieurs jours à des patterns d’activité électrique plus complexe qu’à l’accoutumée. Ceux-ci pourraient par la suite provoquer le déphasage d’autres fonctions physiologiques contribuant aux symptômes du décalage horaire.
On voit donc que d’une horloge biologique centrale unique située dans les noyaux suprachiasmatiques, notre compréhension des rythmes biologiques est passée à un modèle ressemblant à un orchestre où le chef est le NSC et les musiciens l’ensemble des horloges périphériques. Avec l’étude du décalage horaire, on découvre que le NSC lui-même peut être vu comme un ensemble de plusieurs unités fonctionnelles distinctes et interconnectées.
L’horloge biologique serait donc beaucoup plus proche d’un réseau de multiples oscillateurs, certains étant entraînés rapidement par les changement de luminosité, d’autres plus lentement, d’autres encore étant entraînés moins par la lumière que par d’autres facteurs comme la nourriture.